Sikloadisi adalah suatu reaksi kimia perisiklik, ketika dua atau lebih molekul tak jenuh (atau bagian dari molekul yang sama) bergabung dengan pembentukan suatu aduk siklik di mana terdapat reduksi bersih dari multiplisitas ikatannya.Reaksi sikloadisi merupakan reaksi dua molekul bergabung membentuk sebuah cincin. Dalam reaksi ini dua ikatan pi diubah menjadi ikatan sigma. Sikloadisi dibagi menjadi beberapa tipe antara lain sikloadisi [2+2], [4+2], [4+4], [6+2], [6+2], [6+4], dan lain-lain. Dua angka tersebut melambangkan jumlah electron pi yang terlibat dalam suatu reaksi sikloadisi. Berikut ini contoh sederhana reaksi sikloadisi :

jenis sikloadisi
Adapun jenis-jenis sikloadisi adalah sebagai berikut :
- Reaksi Diels-Alder
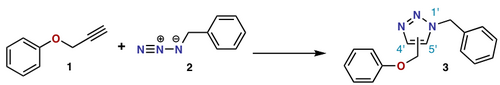
- Sikloadisi Huisgen
- Sikloadisi nitron-olefin
- Sikloadisi olefin 2+2 dikatalisis-besi
- Reaksi keletropik
Reaksi Diels-Alder
Reaksi Diels-Alder mungkin merupakan reaksi sikloadisi yang paling penting dan umum diajarkan. Secara formal reaksi ini merupakan suatu reaksi sikloadisi [4+2] dan hadir dalam berbagai bentuk, termasuk reaksi Diels-Alder heksadehidro dan trimerisasi alkuna terkait. Reaksi juga dapat berjalan dalam arah sebaliknya seperti dalam reaksi retro-Diels–Alder.
Reaksi adisi siklo (Diels Alder) merupakan reaksi antara diena terkonjugasi dengan suatu dienofil. Dalam hal ini, reaksi Diels Alder hanya dapat berlangsung jika diena terkonjugasi tersebut berada dalam bentuk konformasi s-cis. Reaksi ini melibatkan pemutusan satu ikatan π dari diena dan juga satu ikatan ikatan π dienofil. Selain itu, reaksi ini juga melibatkan pembentukan cincin (siklisasi) antara diena dan dienofil, sehingga menghasilkan senyawa siklik, sebagaimana diilustrasikan pada Gambar berikut.
Jika diena terkonjugasi tersebut berada dalam bentuk konformasi s-trans, maka reaksi masih dapat berlangsung dengan bantuan pemanasan. Ikatan tunggal C-C pada diena s-trans dapat mengalami rotasi dengan bantuan pemanasan, sehingga bentuk konformasi s-trans dapat berubah menjadi s-cis, sebagaimana dapat dilihat pada Gambar berikut.
Tidak semua diena terkonjugasi dengan konformasi s-trans dapat berubah menjadi s-cis. Pada sikloalkadiena s-trans dengan salah satu ikatan π berada pada suatu cincin, sedangkan satu ikatan π yang lain berada di luar cincin, rotasi ikatan tidak dapat terjadi, sehinga reaksi Diels Alder tidak dapat berlangsung meskipun sudah dibantu dengan pemanasan. Contoh s-trans alkadiena yang tidak dapat mengalami perubahan konformasi dapat dilihat pada Gambar di bawah ini.
Sikloadisi Huisgen
Sikloadisi nitron-olefin
Sikloadisi nitron-olefin merupakan suatu reaksi sikloadisi (3+2).
Sikloadisi olefin 2+2 dikatalisis-besi
Katalis besi[piridina(diimina)] mengandung ligan aktif redoks dimana pusat atom besi dapat berkoordinasi dengan dua ikatan rangkap dua pada olefin sederhana dan tidak difungsikan. Katalis dapat ditulis sebagai resonansi antara struktur yang mengandung elektron yang tidak berpasangan dengan atom besi pusat dalam keadaan oksidasi II, dan di mana zat besi berada dalam keadaan oksidasi 0. Hal ini memberi fleksibilitas untuk mengikat ikatan rangkap saat mereka menjalani reaksi siklisasi, menghasilkan struktur siklobutana melalui eliminasi reduksi C-C; Sebagai alternatif, struktur siklobutena dapat diproduksi dengan eliminasi beta-hidrogen. Efisiensi reaksi bervariasi tergantung pada alkena yang digunakan, namun desain ligan yang rasional memungkinkan perluasan kisaran reaksi yang dapat dikatalisis.
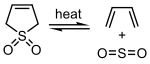
Reaksi keletropik
Reaksi keletropik adalah suatu subkelas sikloadisi. Fitur pembeda utama dari reaksi keletropik adalah bahwa pada salah satu pereaksi, kedua ikatan baru dibuat pada atom yang sama. Contoh klasiknya adalah reaksi belerang dioksida dengan diena.